(北欧时报斯德哥尔摩讯 记者何儒 特约记者李薛鑫、朱文韬、罗冉报道)10月2日中午12时,瑞典卡罗林斯卡医学院,将2023年诺贝尔生理学或医学奖授予匈牙利科学家卡塔琳·考里科和德鲁·韦斯曼,理由是他们在信使核糖核酸(mRNA)研究上的突破性发现,这些发现助力疫苗开发达到前所未有的速度。
评奖委员会在新闻公报中说,两位获奖者的研究成果“从根本上改变了对mRNA如何与免疫系统相互作用的理解”,对于在新冠疫情期间开发有效的mRNA疫苗至关重要。在现代人类健康面临威胁时,获奖者的研究为疫苗前所未有的开发速度做出了重要贡献。
评奖委员会说,生产基于全病毒、病毒蛋白质和病毒载体的疫苗需要大规模细胞培养,其资源密集型过程限制了疫情暴发时快速生产疫苗的可能性。与病毒基因片段相对应的mRNA可以让机体细胞生成病毒的蛋白,从而激发免疫反应,因而也可以作为疫苗候选,但细胞外生产的mRNA依然不稳定且传递效果差。
两位获奖者研究发现,只要对细胞外生产的mRNA进行核苷酸碱基修饰,就可以让机体将外源mRNA“识别”为自身的mRNA,递送后既能减少炎症反应又能增加蛋白质产量。这一成果消除了mRNA临床应用道路上的关键障碍,开发mRNA疫苗的灵活性和速度为针对其他传染病疫苗的开发铺平了道路。未来该技术还可用于输送治疗性的蛋白质并治疗某些癌症类型。
考里科1955年出生于匈牙利的索尔诺克,现任匈牙利塞格德大学教授和美国宾夕法尼亚大学佩雷尔曼医学院兼职教授。韦斯曼1959年出生于美国马萨诸塞州,现任宾夕法尼亚大学RNA创新研究所所长。
评奖委员会秘书托马斯·佩尔曼在当天举行的新闻发布会上表示,他已经与获奖者们取得电话联系,考里科听到消息感到“不知所措”,而韦斯曼表示“很高兴能获奖”。
两位获奖者将平分1100万瑞典克朗(约合100万美元)奖金。
发布会现场,北欧时报获得提问机会。
北欧时报记者:谢谢主席,我是《北欧时报》记者。很高兴再次出席新闻发布会,去年我曾在这个位置提出同样的问题。就是关于mRNA技术在新冠疫苗中发挥的重要作用,很遗憾去年落选了,而今天终于把这一荣誉授予他们,真乃实至名归,我相信每个人都对此感到高兴。
我的第一个问题是涉及mRNA疫苗。在癌症或传染病等其他疾病方面,mRNA疫苗在其他领域有哪些潜在应用?如有,能否为我们进一步阐述?
第二个问题涉及COVID-19的长期影响,我认为这对社会非常重要。您能否分享一些相关见解?
诺奖委员会主席答:
关于其他应用,目前正在这一领域进行了大量的研究,考虑到平台上的丰富数据,这一趋势可能会持续下去。我们预计的主要应用包括开发针对传染性疾病的各种疫苗。例如,有可能开发针对流感等感染病的疫苗,需要定期更新。这个平台的主要优势之一是其灵活性和速度,允许对新病毒变种迅速进行疫苗更新,而这在流感中是常见的情况。
此外,还有其他应用正在探索中,可能不会立即激动人心,但在治疗和疫苗方面具有潜力。这些治疗通常不是预防性的,可以根据个体需求进行定制,也可以以更普遍的方式应用。癌症是一种复杂而具有挑战性的疾病,有多种形式,这种方法可能会在很大程度上受益于癌症。
此外,已经进行了许多实验和临床试验,以传递治疗性蛋白质,这可能涉及替换有缺陷的酶或引入免疫调节蛋白质。因此,我们预计将见证大量的研究工作应用于各种疾病。
至于您提出的关于长期COVID-19的第二部分问题,首先,疫苗在预防COVID-19感染方面起着至关重要的作用。长期COVID包括一系列不同的症状,从轻微的症状到更严重的表现不一而足。值得注意的是,与接种疫苗的人群相比,感染了病毒的人更容易患上长期COVID。然而,长期COVID的严重程度和持续性原因仍然不明确。研究人员正在积极调查这一现象,我相信持续的研究将为这个复杂的问题带来更多的启示。
发布会现场。/图 北欧时报 朱文韬
发布会后,北欧时报专访诺贝尔医学或生理学奖评委,瑞典卡罗林斯卡大学潘嫱教授,她也是今年唯一一位晋升到医学或生理学奖评委的华人女院士。
北欧时报记者:潘教授,您好。我是北欧时报记者,非常感谢您接受我们的采访。鉴于新冠病毒不断发生变异,请问是否有必要进一步改进和优化基于mRNA的疫苗技术,以更好地应对这些变异?
潘嫱教授回答:当前,全球范围内对COVID-19的mRNA疫苗持续进行研究,同时,mRNA技术的灵活性为我们有效抵抗新冠变种提供了重要支持。然而,值得注意的是,mRNA疫苗技术目前仍处于不断发展和优化的阶段。根据我们的研究发现,新冠病毒变种主要通过上呼吸道传播,而在免疫系统激活过程中,免疫球蛋白IgA发挥着关键作用。然而,通过肌肉注射的mRNA疫苗并不能引发足够高水平的IgA反应。因此,一种新型的粘膜给药方式被提出,以更有效地激发免疫反应。
总的来说,现阶段,无论是疫苗本身还是给药方式,相关研究都在积极进行中。尽管相较于2020年,我们已经取得了明显进展,这要感谢今年这两位获奖科学家,和众多科学家及制药公司的辛勤努力,但仍然需要不断改进。科学家和公司已经在疫情中积累了丰富经验,拥有更多资源,因此能够投入更多资金进行研究。我们对未来充满信心,感谢这些科学家们的不懈努力。
谢谢!
获奖简介
The2023Nobel Prize in Physiology or Medicine
jointly to
Katalin Karikóand Drew Weissman
两位诺贝尔奖得主的发现对于在2020年初开始的大流行期间开发出针对COVID-19的有效mRNA疫苗至关重要。通过他们开创性的研究,彻底改变了我们对mRNA如何与免疫系统互动的理解,这两位学者为现代人类面临的最大健康威胁之一期间前所未有的疫苗开发速度做出了贡献。
大流行之前的疫苗 疫苗接种刺激对特定病原体形成免疫反应,这使身体在日后再次接触时能够更快地与疾病作斗争。基于杀死或减弱病毒的疫苗早已可用,小儿麻痹症、麻疹和黄热病的疫苗就是例证。1951年,Max Theiler因开发黄热病疫苗而获得诺贝尔生理学或医学奖。
得益于近几十年来分子生物学的进步,基于单个病毒组件而非整个病毒的疫苗已经被开发出来。通常编码在病毒表面上的蛋白质的病毒遗传编码的部分被用来制造刺激生成抗病毒抗体的蛋白质。例如乙肝和人乳头瘤病毒的疫苗。或者,病毒遗传编码的部分可以转移到无害的载体病毒(“载体”)上。这种方法用于埃博拉病毒的疫苗。当载体疫苗注射时,我们细胞中会产生所选的病毒蛋白,刺激针对目标病毒的免疫反应。
生产全病毒、蛋白质和载体基疫苗需要大规模的细胞培养。这种资源密集型的过程限制了快速响应疫情和大流行病的疫苗生产的可能性。因此,研究人员长期以来一直试图开发独立于细胞培养的疫苗技术,但这被证明是具有挑战性的。
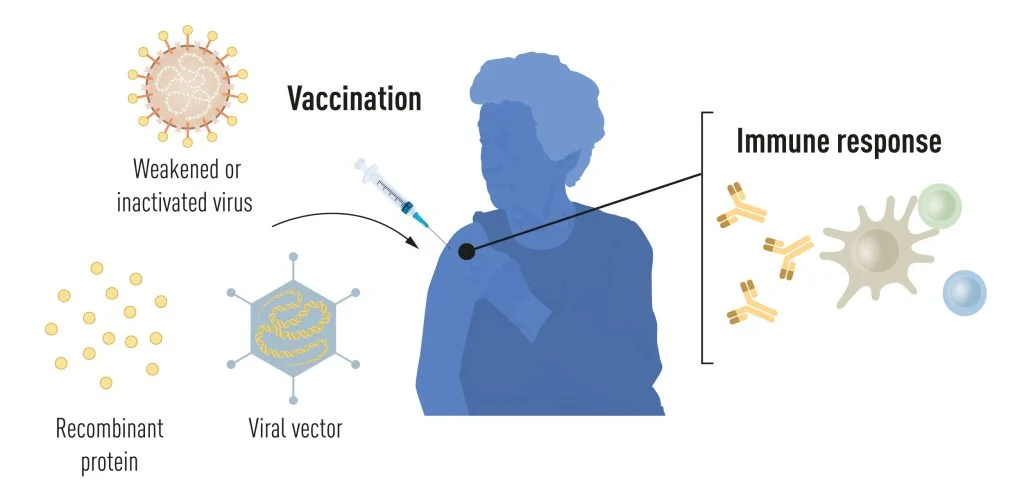
mRNA疫苗:一个有希望的想法在我们的细胞中,DNA中编码的遗传信息被转移到信使RNA(mRNA)上,mRNA用作蛋白质生产的模板。在1980年代,介绍了一种无需细胞培养即可有效生产mRNA的方法,称为体外转录。这一决定性步骤加速了分子生物学在多个领域的应用发展。使用mRNA技术进行疫苗和治疗用途的想法也开始兴起,但前方仍存在障碍。体外转录的mRNA被认为是不稳定且难以传递的,需要开发复杂的载体脂质系统来包裹mRNA。此外,体外生产的mRNA会导致炎症反应。因此,最初对将mRNA技术用于临床目的的热情是有限的。这些障碍并没有阻止匈牙利生物化学家Katalin Karikó,她致力于开发使用mRNA进行治疗的方法。在1990年代初,当她在宾夕法尼亚大学担任助理教授时,尽管在说服研究资助者重视她的项目方面遇到了困难,但她仍然坚持实现mRNA作为治疗的想法。卡里克奥在该大学的一名新同事是免疫学家德鲁·韦斯曼博士。他对树突状细胞感兴趣,这些细胞在免疫监视和疫苗诱导的免疫应答激活中起重要作用。在新思想的刺激下,两人很快就开始了富有成效的合作,专注于不同类型的RNA如何与免疫系统相互作用。
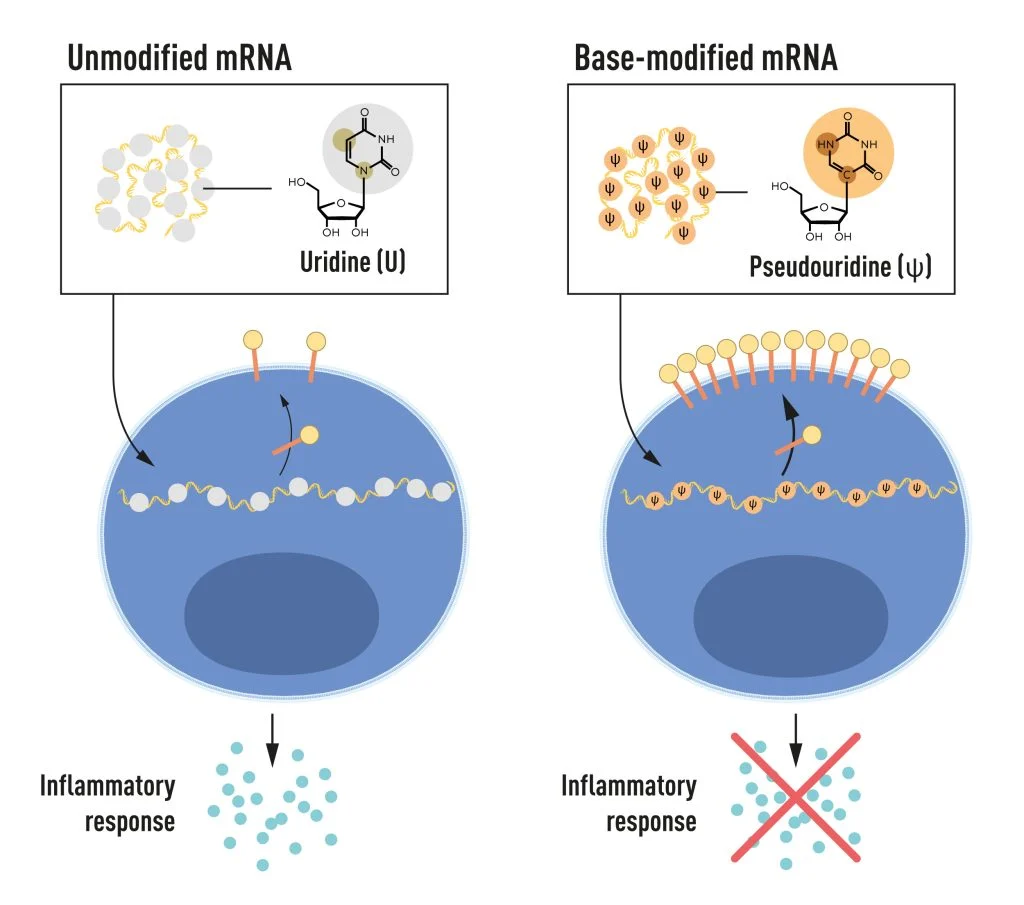
Karikó和Weissman注意到树突状细胞将体外转录的mRNA识别为外来物质,导致它们的激活和炎症信号分子的释放。他们想知道为什么体外转录的mRNA被识别为外来物质,而来自哺乳动物细胞的mRNA则没有引起同样的反应。Karikó和Weissman意识到某些关键性质必须区分不同类型的mRNA。RNA包含四个碱基,缩写为A、U、G和C,对应于DNA中的遗传密码字母A、T、G和C。Karikó和Weissman知道来自哺乳动物细胞的RNA中的碱基经常进行化学修饰,而体外转录的mRNA则没有。他们想知道体外转录的RNA中缺少经过修饰的碱基是否能够解释不受欢迎的炎症反应。为了研究这个问题,他们生产了具有不同化学修饰变体的mRNA的不同变体,并将它们输送到树突状细胞。结果令人惊讶:当在mRNA中包括碱基修饰时,炎症反应几乎完全消失。这是我们对细胞如何识别和应对不同形式的mRNA的理解发生了范式性转变。Karikó和Weissman立即认识到他们的发现对于将mRNA用作治疗具有重要意义。这些开创性的结果在2005年发表,比COVID-19大流行提前十五年。
在2008年和2010年发表的进一步研究中,Karikó和Weissman表明,使用经过碱基修饰生成的mRNA显著提高了蛋白质产量,这要归功于调节蛋白质生产的酶的活性降低。通过他们的发现,碱基修饰既减少了炎症反应又增加了蛋白质产量,Karikó和Weissman消除了将mRNA应用于临床的巨大障碍。mRNA疫苗实现了潜力对mRNA技术的兴趣开始增加,2010年,几家公司致力于开发该方法。针对寨卡病毒和MERS-CoV的疫苗被追求;后者与SARS-CoV-2密切相关。在COVID-19大流行爆发后,以两种基于SARS-CoV-2表面蛋白的经碱基修饰的mRNA为基础,疫苗以创纪录的速度被开发出来。据报道保护效果约为95%,这两种疫苗最早在2020年12月获得批准。
mRNA疫苗可以以令人印象深刻的灵活性和速度进行开发,为利用这一新平台来开发其他传染病的疫苗铺平了道路。在未来,该技术还可能用于输送治疗性蛋白质和治疗某些癌症类型。基于不同方法的其他几种针对SARS-CoV-2的疫苗也迅速推出,全球共提供了超过130亿剂COVID-19疫苗。这些疫苗挽救了数百万人的生命并防止了许多更严重的疾病,使社会能够开放并恢复正常状态。通过他们对碱基修饰在mRNA中的重要性的基本发现,今年的诺贝尔奖得主对这个在我们这个时代最大的健康危机期间的转型性发展做出了重要贡献。
Key publications
Karikó,K.,Buckstein,M.,Ni,H.and Weissman,D.Suppression of RNA Recognition by Toll-like Receptors:The impact of nucleoside modification and the evolutionary origin of RNA. Immunity 23,165–175(2005).
Karikó,K.,Muramatsu,H.,Welsh,F.A.,Ludwig,J.,Kato,H.,Akira,S.and Weissman,D.Incorporation of pseudouridine into mRNA yields superior nonimmunogenic vector with increased translational capacity and biological stability. Mol Ther 16,1833–1840(2008).
Anderson,B.R.,Muramatsu,H.,Nallagatla,S.R.,Bevilacqua,P.C.,Sansing,L.H.,Weissman,D.and Karikó,K.Incorporation of pseudouridine into mRNA enhances translation by diminishing PKR activation. Nucleic Acids Res. 38,5884–5892(2010).
/编审 何儒







